Chiến lược kiểm soát Acinetobacter baumannii MDR bằng giám sát chủ động
- Lỗ hổng Chăm sóc Y tế và Nghịch lý của Y học Hiện đại qua Sự kiện tại Thụy Sĩ
- Đặc điểm Sinh lý Bệnh học của Nhiễm trùng Acinetobacter baumannii ở Bệnh nhân Bỏng
- Sự Phá vỡ Hàng rào Bảo vệ Vô cơ và Môi trường Vi sinh tại Vết Bỏng
- Hội chứng Đáp ứng Viêm Hệ thống và Sự "Tê liệt" Miễn dịch
- Độc lực Tế bào: Khả năng Hình thành Màng sinh học và Sự Bền bỉ trong Môi trường
- Cuộc Khủng hoảng Kháng thuốc và Sự Giới hạn của Các Lựa chọn Điều trị
- Phân tích Danh sách Tác nhân Ưu tiên từ Tổ chức Y tế Thế giới (WHO 2024)
- Phân tích Dữ liệu Kháng thuốc từ ECDC (2022)
- Tác động Xúc tác của Đại dịch COVID-19 (Dữ liệu CDC 2022)
- Nút thắt Chẩn đoán và Bước đột phá của Môi trường Nuôi cấy Sinh màu (CHROMagar™)
- Chiến dịch Xóa sổ Kháng thuốc Ngoạn mục tại Chapel Hill (2008)
- Kết luận và Đề xuất Khung Chiến lược Quản trị Rủi ro Sinh học
Báo cáo nghiên cứu về Acinetobacter baumannii đa kháng thuốc cung cấp cái nhìn chuyên sâu về cơ chế bệnh sinh, thực trạng dịch tễ học toàn cầu và các giải pháp giám sát chủ động bằng công nghệ sinh học tại đơn vị hồi sức tích cực.
Lỗ hổng Chăm sóc Y tế và Nghịch lý của Y học Hiện đại qua Sự kiện tại Thụy Sĩ
Sự tiến bộ vượt bậc của y học hiện đại trong lĩnh vực hồi sức cấp cứu và điều trị chấn thương đã cho phép duy trì sự sống cho những bệnh nhân nguy kịch nhất, vượt qua ranh giới của tỷ lệ tử vong từng được coi là tất yếu trong quá khứ. Tuy nhiên, chính không gian được thiết kế với tiêu chuẩn vô trùng khắt khe nhất để chữa lành lại đang dần trở thành một hệ sinh thái lý tưởng cho sự tiến hóa và bùng phát của những mầm bệnh nguy hiểm bậc nhất. Nghịch lý tàn khốc này đã được phơi bày một cách bi thảm thông qua sự kiện một bệnh nhân 18 tuổi, nạn nhân sống sót sau vụ cháy rừng thảm khốc tại Crans-Montana, đã tử vong tại Bệnh viện Đại học Zürich (USZ) ở Thụy Sĩ. Theo báo cáo điều tra của Hässig, L. (2026), nguyên nhân trực tiếp dẫn đến cái chết của bệnh nhân trẻ tuổi này không phải do những di chứng từ các vết bỏng nhiệt sâu hay sự suy kiệt do thảm họa thiên nhiên, mà là do một đợt nhiễm khuẩn bệnh viện (Healthcare-Associated Infection - HAI) gây ra bởi chủng vi khuẩn Acinetobacter baumannii đa kháng thuốc (MDR).1
Sự kiện chấn động tại Thụy Sĩ không nên được nhìn nhận như một hiện tượng đơn lẻ hay một tai nạn y khoa ngẫu nhiên. Ngược lại, nó là bề nổi của một cuộc khủng hoảng dịch tễ học mang tính hệ thống đang đe dọa sự bền vững của các hệ thống y tế trên toàn cầu. Chỉ tính riêng tại Thụy Sĩ, dữ liệu thống kê hàng năm ghi nhận khoảng 70.000 ca bệnh nhân mắc phải các bệnh lý nhiễm khuẩn ngay trong thời gian lưu trú tại bệnh viện, dẫn đến sự ra đi của xấp xỉ 5.900 người.2 Mặc dù các mầm bệnh này hiếm khi là nguyên nhân duy nhất gây tử vong mà thường đóng vai trò là giọt nước tràn ly trên nền thể trạng đã suy kiệt của bệnh nhân, nhưng tổn thất sinh mạng khổng lồ này vẫn là một hồi chuông cảnh báo không thể phớt lờ. Đáng chú ý, các chuyên gia dịch tễ học từ Trung tâm Quốc gia về Phòng ngừa Nhiễm khuẩn Swissnoso, điển hình như chuyên gia Walter Zingg, và Văn phòng Y tế Công cộng Liên bang (BAG) đã liên tục đưa ra các báo cáo phân tích rủi ro, nhấn mạnh rằng khoảng một nửa số ca nhiễm khuẩn bệnh viện hoàn toàn có thể phòng ngừa được nếu hệ thống giám sát hoạt động hiệu quả.3
Tuy nhiên, những cảnh báo cấp bách này dường như chưa được Hội đồng Liên bang (Bundesrat) và ban lãnh đạo các bệnh viện chuyển hóa thành các biện pháp can thiệp đủ mạnh tay tại các cơ sở điều trị tích cực (ICU). Những nỗ lực lập pháp và chính sách, từ đề xuất năm 2012 của Nghị sĩ Edith Graf-Litscher cho đến những tuyên bố lặp lại vào năm 2023, vẫn vấp phải sự trễ nải trong khâu thực thi thực tiễn.3 Việc một nạn nhân bỏng sống sót qua ngọn lửa tàn khốc nhưng lại gục ngã trước một vi sinh vật vô hình ngay trong một trung tâm y tế hàng đầu của Châu Âu đã đặt ra những câu hỏi nền tảng về quy trình kiểm soát nhiễm khuẩn, sự phân bổ nguồn lực chẩn đoán, và triết lý quản trị rủi ro sinh học tại bệnh viện.4 Cái chết này nhấn mạnh một lỗ hổng chí mạng trong khả năng phát hiện sớm và cách ly nguồn lây nhiễm A. baumannii. Sự sống còn của bệnh nhân giờ đây không chỉ phụ thuộc vào kỹ thuật ghép da hay máy thở tuần hoàn, mà phụ thuộc hoàn toàn vào tốc độ và độ nhạy của hệ thống giám sát vi sinh lâm sàng tại cơ sở điều trị.
Đặc điểm Sinh lý Bệnh học của Nhiễm trùng Acinetobacter baumannii ở Bệnh nhân Bỏng
Để thấu hiểu cơ chế vì sao nạn nhân cháy rừng Crans-Montana lại trở thành mục tiêu tấn công hoàn hảo của A. baumannii, cần phải tiến hành một phân tích sâu sắc về những biến đổi sinh lý bệnh học phức tạp xảy ra sau chấn thương bỏng nặng. Tổn thương bỏng không chỉ đơn thuần là sự phá hủy lớp rào chắn vật lý bảo vệ cơ thể, mà nó khởi phát một chuỗi các phản ứng suy giảm miễn dịch mang tính hệ thống, biến bệnh nhân thành một "môi trường nuôi cấy" sinh học lý tưởng cho các vi khuẩn cơ hội.
Sự Phá vỡ Hàng rào Bảo vệ Vô cơ và Môi trường Vi sinh tại Vết Bỏng
Lớp biểu bì và hạ bì của con người khi ở trạng thái khỏe mạnh đóng vai trò như một pháo đài sinh học, ngăn chặn sự xâm nhập của hàng tỷ vi sinh vật tồn tại trong môi trường xung quanh. Khi lớp rào chắn này bị phá hủy hoàn toàn bởi nhiệt độ cao, các mô hoại tử (eschar) kết hợp với lượng lớn dịch tiết giàu protein tạo thành một môi trường dồi dào chất dinh dưỡng cho vi khuẩn.5A. baumannii là một trực khuẩn Gram âm hiếu khí, đa hình thái, có đặc tính nội tại cực kỳ nguy hiểm là khả năng tồn tại dai dẳng trong cả môi trường khô hạn lẫn môi trường ẩm ướt.7 Mầm bệnh này nhanh chóng tận dụng lợi thế của các vùng mô tổn thương để xâm nhập, định cư và phát triển theo cấp số nhân. Ở những bệnh nhân có diện tích bề mặt cơ thể bị bỏng lớn (Total Body Surface Area - TBSA > 10%), nguy cơ nhiễm trùng máu và nhiễm trùng đa cơ quan tăng vọt do mạng lưới mao mạch bị bộc lộ trực tiếp với vi khuẩn từ môi trường ngoài.5 Dữ liệu lâm sàng chỉ ra rằng có một sự tương quan nghịch biến rõ rệt giữa diện tích TBSA bị tổn thương và tiên lượng sống sót, chủ yếu do rủi ro nhiễm khuẩn huyết thứ phát.5
Hội chứng Đáp ứng Viêm Hệ thống và Sự "Tê liệt" Miễn dịch
Song song với tổn thương tại chỗ, chấn thương bỏng diện rộng là chất xúc tác mạnh mẽ nhất kích hoạt Hội chứng Đáp ứng Viêm Hệ thống (Systemic Inflammatory Response Syndrome - SIRS), kéo theo sau đó là Hội chứng Đáp ứng Chống viêm Bù trừ (Compensatory Anti-inflammatory Response Syndrome - CARS).6 Sự giải phóng ồ ạt các cytokine tiền viêm và sự mất cân bằng trong điều hòa miễn dịch gây ra tình trạng "tê liệt miễn dịch" toàn thân. Tình trạng này làm suy yếu nghiêm trọng chức năng thực bào của đại thực bào, giảm khả năng hóa ứng động của bạch cầu trung tính và làm suy kiệt hệ thống tế bào lympho T và B.6
Khi tình trạng ức chế miễn dịch này kết hợp với các tổn thương đường hô hấp do hít phải khói độc (inhalation injury) – một biến chứng cực kỳ phổ biến trong các vụ cháy rừng như tại Crans-Montana – rủi ro tử vong do các đợt tấn công của A. baumannii tăng lên gấp nhiều lần.5 Khói độc bào mòn hệ thống lông chuyển niêm mạc phế quản, mở đường cho vi khuẩn xâm nhập sâu vào nhu mô phổi. Thực tế lâm sàng tại các đơn vị bỏng tích cực (BICU) cho thấy vi khuẩn này thường là thủ phạm chính gây ra các biến chứng chết người như viêm phổi liên quan đến thở máy (VAP), nhiễm khuẩn huyết, và nhiễm trùng tiểu.7 Vi khuẩn này thường tận dụng các thiết bị y tế xâm lấn như ống nội khí quản, ống thông tĩnh mạch trung tâm, và catheter đường tiết niệu làm cửa ngõ để xâm nhập vào tuần hoàn trung tâm.9
Độc lực Tế bào: Khả năng Hình thành Màng sinh học và Sự Bền bỉ trong Môi trường
Một trong những yếu tố độc lực tiến hóa nguy hiểm nhất của A. baumannii là khả năng hình thành màng sinh học (biofilm) cực kỳ vững chắc trên cả bề mặt mô sống và các vật liệu phi sinh học như nhựa, silicon và kim loại.6 Màng sinh học này được cấu thành từ một lớp vỏ polymer ngoại bào (Extracellular Polymeric Substances - EPS), hoạt động như một lá chắn vật lý và hóa học, bảo vệ cộng đồng vi khuẩn bên trong khỏi sự tấn công của các tế bào bạch cầu cũng như sự thẩm thấu của các tác nhân kháng sinh thông thường.
Khả năng bám dính siêu việt này cho phép A. baumannii tồn tại dai dẳng trên các thiết bị y tế dùng chung như máy thở, thành giường bệnh, màn hình theo dõi sinh hiệu, và thậm chí là các thiết bị làm mát cơ học như quạt bàn trong suốt nhiều tuần lễ, chờ đợi cơ hội tiếp xúc với vật chủ suy giảm miễn dịch.7 Đặc tính sinh tồn bất chấp các chu trình khử khuẩn hóa chất thông thường này giải thích lý do tại sao các đợt bùng phát (outbreak) A. baumannii nội viện thường mang tính dây chuyền, cực kỳ khó kiểm soát triệt để, và đòi hỏi những biện pháp can thiệp vượt xa các tiêu chuẩn vệ sinh thông thường.11
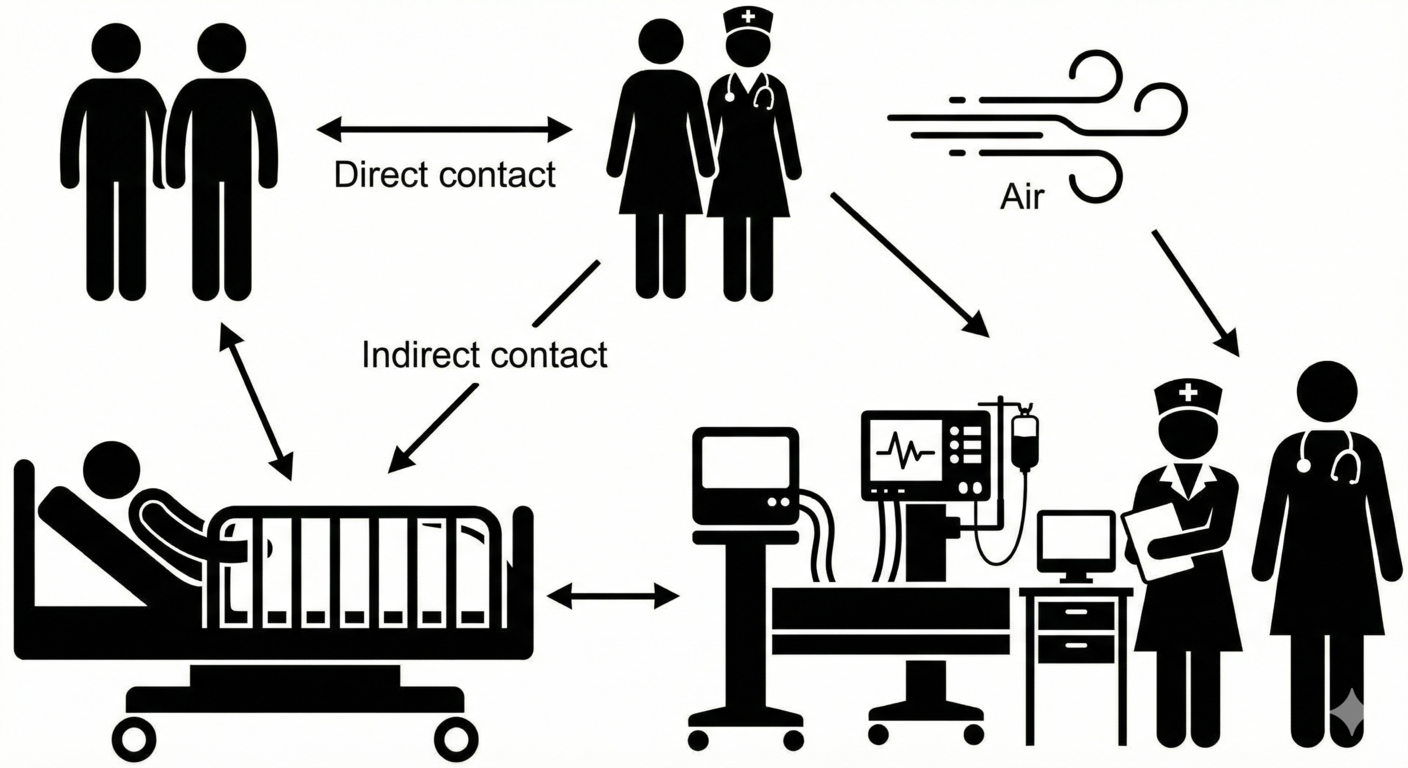
Hình 1. Chuỗi lây truyền dịch tễ học của mầm bệnh trong không gian chăm sóc tích cực (ICU). Mô hình trực quan hóa các con đường lây nhiễm chéo nội viện, từ tiếp xúc trực tiếp giữa các bệnh nhân, truyền lây qua trung gian là nhân viên y tế, cho đến các vector cơ học như bề mặt thiết bị y tế và lây truyền qua đường không khí.
Cuộc Khủng hoảng Kháng thuốc và Sự Giới hạn của Các Lựa chọn Điều trị
Sự lây nhiễm của A. baumannii sẽ không trở thành một bản án tử hình nếu vi khuẩn này vẫn nhạy cảm với các liệu pháp kháng sinh truyền thống. Tuy nhiên, qua nhiều thập kỷ tiếp xúc với áp lực chọn lọc từ môi trường bệnh viện, mầm bệnh này đã tiến hóa thành một cỗ máy đa kháng thuốc (MDR) hoàn hảo.11 Các chủng MDR Acinetobacter được định nghĩa là có khả năng kháng lại hoặc giảm độ nhạy cảm trung gian với từ ba lớp kháng sinh phổ biến trở lên, bao gồm Cephalosporin thế hệ 3, Fluoroquinolone, và đặc biệt là Carbapenem – vốn được coi là "tuyến phòng thủ cuối cùng" của kháng sinh phổ rộng.8
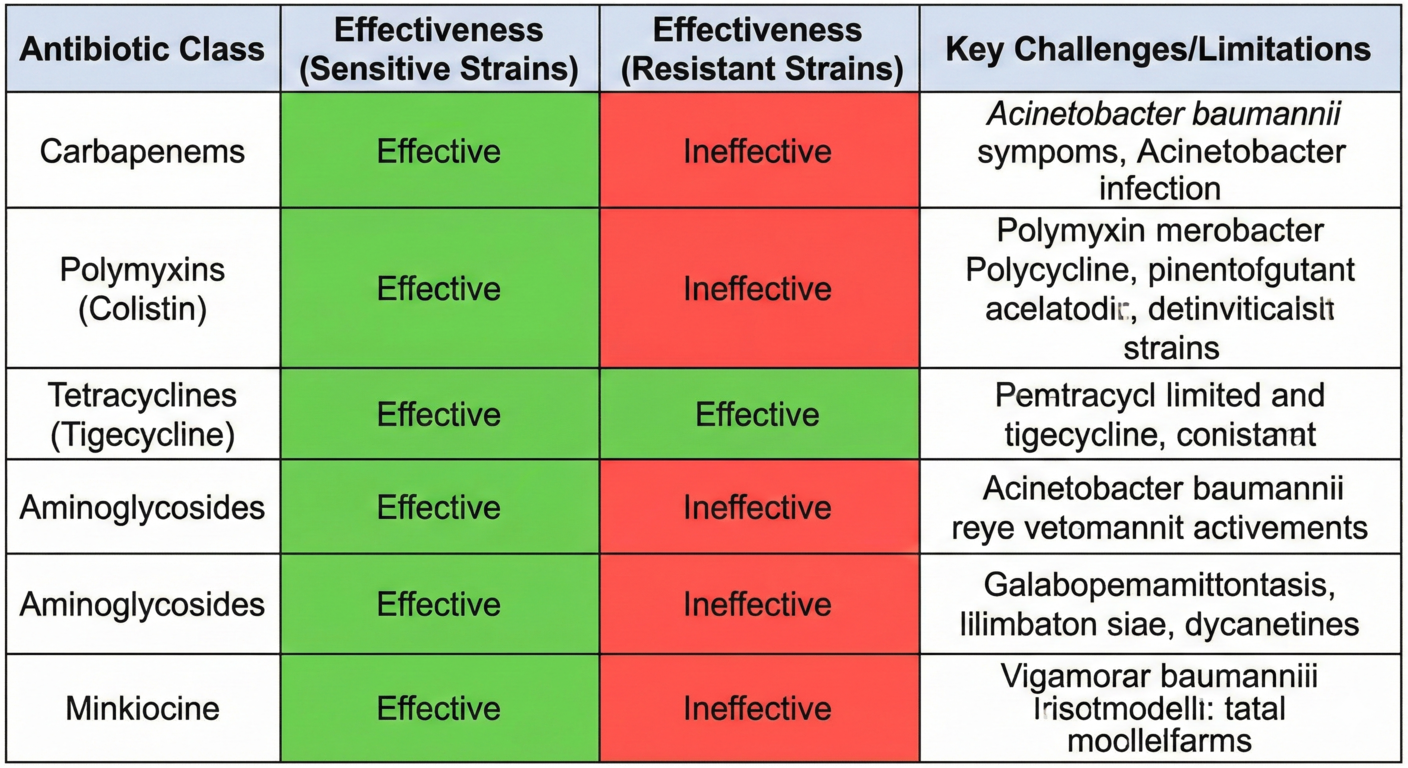
Bảng 1. Bảng đối chiếu phổ tác dụng và hạn chế lâm sàng của các nhóm kháng sinh.
Cơ chế kháng Carbapenem của A. baumannii rất đa dạng và phức tạp, bao gồm việc sản xuất các enzyme phân hủy kháng sinh như carbapenemase loại OXA và metallo-beta-lactamase, cấu trúc lại các kênh porin trên màng ngoài tế bào để ngăn kháng sinh thẩm thấu, và gia tăng biểu hiện của các bơm tống thuốc (efflux pumps) đẩy kháng sinh ra ngoài tế bào trước khi chúng kịp phát huy tác dụng.6 Khi các dòng kháng sinh hiện đại bị vô hiệu hóa, các bác sĩ lâm sàng tại các đơn vị bỏng và ICU thường bị dồn vào thế chân tường, buộc phải sử dụng lại các loại kháng sinh đã lỗi thời và có độc tính cao như Colistin (Polymyxin E).9 Mặc dù trong một số nghiên cứu hồi cứu tại các trung tâm bỏng, việc sử dụng Colistin có thể mang lại tỷ lệ chữa khỏi về mặt lâm sàng lên tới 70%, nhưng tỷ lệ tử vong liên quan trực tiếp đến nhiễm trùng vẫn neo ở mức rất cao (khoảng 30%), chưa kể đến những tổn thương không thể phục hồi đối với chức năng thận và thần kinh của bệnh nhân.9 Sự bế tắc trong phác đồ điều trị này nhấn mạnh rằng, một khi bệnh nhân bỏng đã bị vi khuẩn xâm chiếm, mọi nỗ lực cứu chữa đều đi kèm với rủi ro tử vong cực lớn.
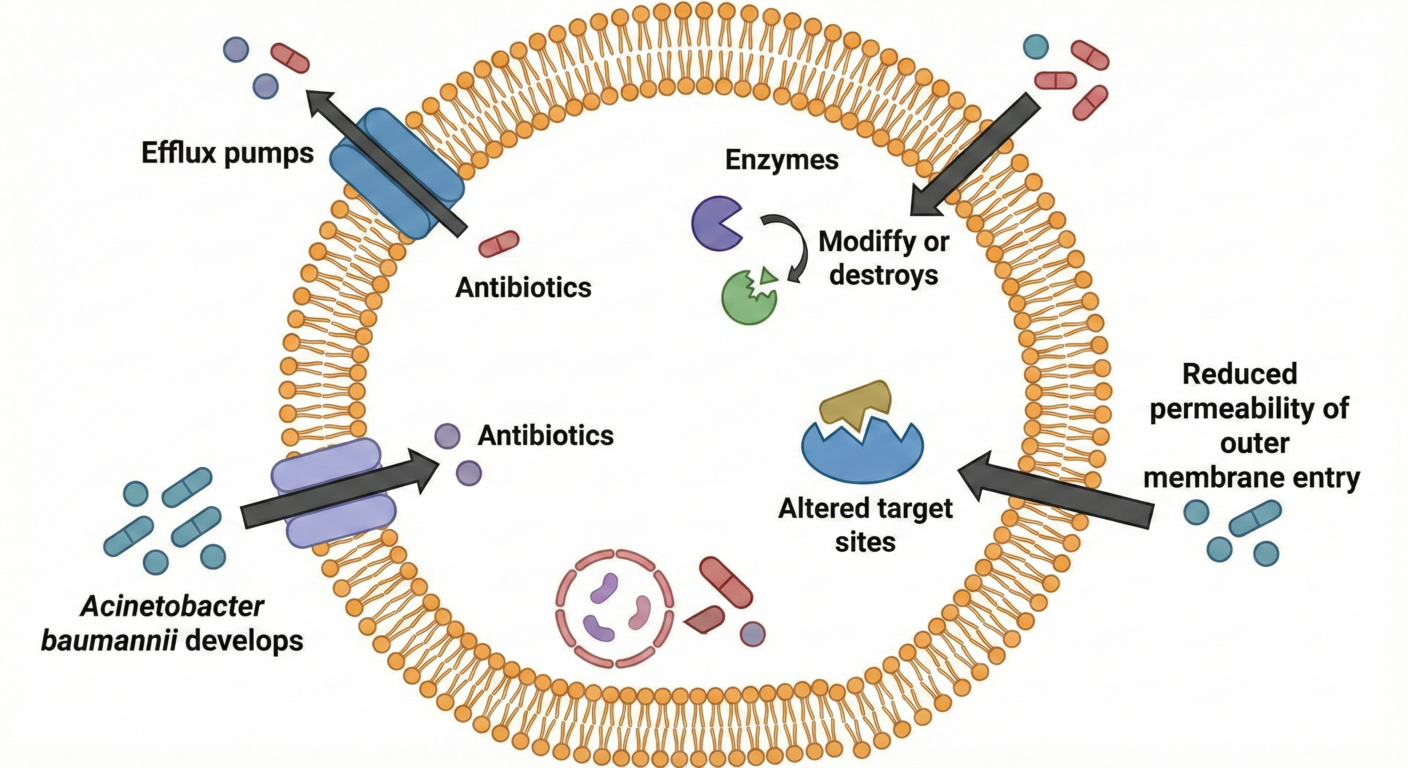
Hình 2. Sơ đồ các cơ chế kháng kháng sinh ở cấp độ tế bào của Acinetobacter baumannii. Hình ảnh minh họa chi tiết các rào cản sinh học giúp vi khuẩn vô hiệu hóa kháng sinh, bao gồm việc sản xuất enzyme phân hủy thuốc, hệ thống bơm tống thuốc (efflux pumps) đẩy kháng sinh ra ngoài, biến đổi đích tác dụng và giảm tính thấm của màng ngoài.
Phân tích Danh sách Tác nhân Ưu tiên từ Tổ chức Y tế Thế giới (WHO 2024)
Sự nguy hiểm và tính chất tàn phá của A. baumannii không chỉ giới hạn trong phạm vi một khoa điều trị bỏng hay một quốc gia cụ thể. Mức độ đe dọa mang tính hiện sinh của mầm bệnh này đối với y tế công cộng đã được hệ thống hóa, lượng hóa và công bố ở cấp độ toàn cầu. Danh sách Tác nhân Gây bệnh Ưu tiên của Vi khuẩn năm 2024 (Bacterial Priority Pathogens List - BPPL) do Tổ chức Y tế Thế giới (WHO) biên soạn cung cấp một khuôn khổ phân tích chiến lược, xác định rõ ràng sự dịch chuyển của cuộc chiến chống kháng thuốc (AMR) trong thế kỷ 21.15
Được xây dựng dựa trên nền tảng của ấn bản năm 2017, WHO BPPL 2024 sử dụng mô hình Phân tích Quyết định Đa tiêu chí (Multi-Criteria Decision Analysis - MCDA) vô cùng nghiêm ngặt.15 Quá trình này được hỗ trợ bởi các dữ liệu cập nhật từ các nghiên cứu đánh giá hệ thống, ước tính gánh nặng bệnh tật toàn cầu do AMR, và các vòng khảo sát chuyên gia đa ngành.16 Cấu trúc phân tích đánh giá các vi khuẩn dựa trên tính lây truyền, khả năng điều trị bằng các phác đồ hiện có, tỷ lệ tử vong, các tùy chọn phòng ngừa (như vắc-xin và kiểm soát nhiễm khuẩn), cũng như tình trạng của đường ống nghiên cứu và phát triển (R&D) các liệu pháp mới.15
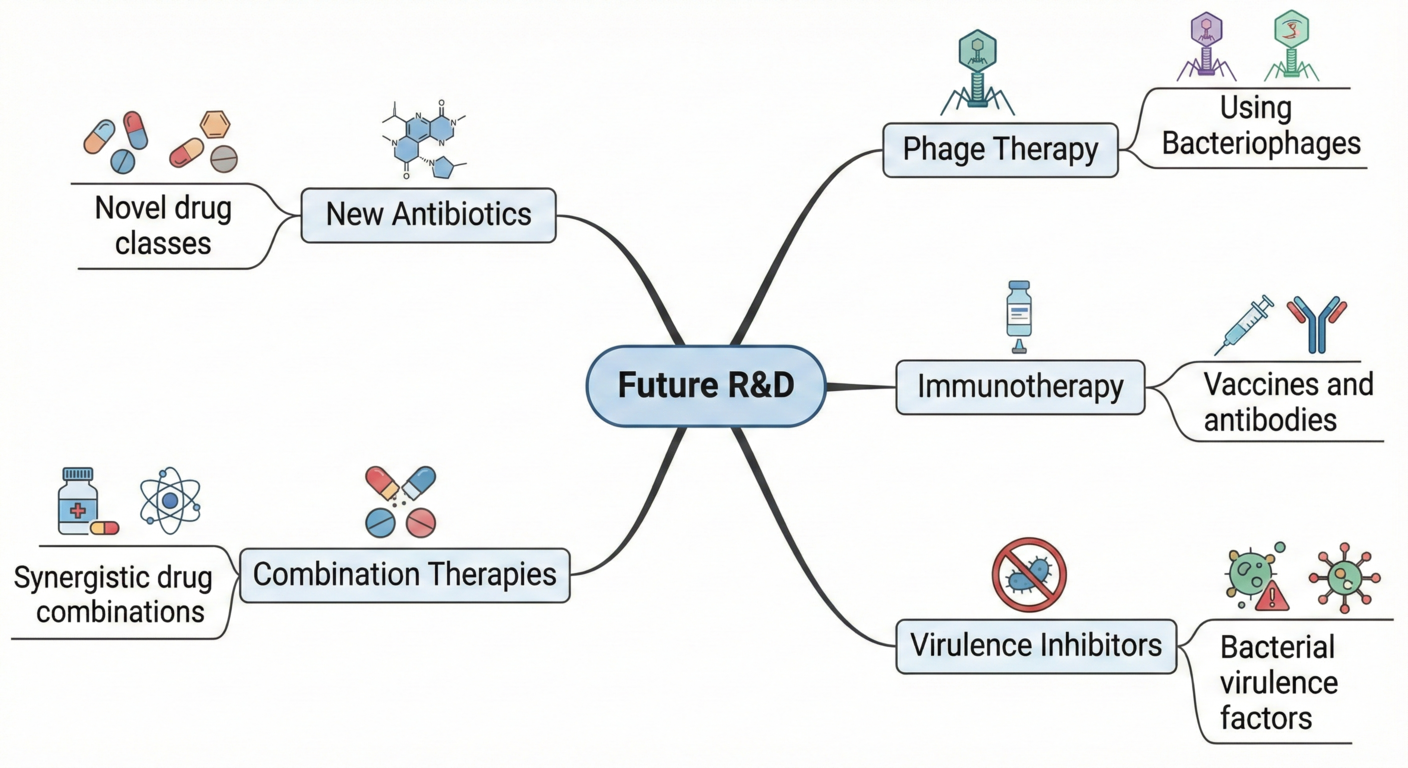
Hình 3. Lộ trình Nghiên cứu và Phát triển (R&D) các nền tảng trị liệu thế hệ mới. Sơ đồ tư duy mở rộng về các định hướng y học tương lai nhằm vượt qua sự bế tắc của kháng sinh truyền thống, nhấn mạnh vào liệu pháp thể thực khuẩn (Phage Therapy), kháng thể miễn dịch, thuốc kết hợp và các chất ức chế độc lực chọn lọc.
Trong danh sách bao gồm 24 mầm bệnh mục tiêu trải dài qua 15 họ vi khuẩn kháng thuốc, Acinetobacter baumannii kháng Carbapenem (CRAB) được xếp hạng ở vị trí cao nhất trong nhóm "Ưu tiên Đặc biệt Khẩn cấp" (Critical Priority).15 Đây là mức cảnh báo tột cùng, dành riêng cho các tác nhân vi khuẩn đe dọa trực tiếp và tức thời đến sinh mạng con người, đòi hỏi sự can thiệp từ cấp độ chính phủ và tập trung ngân sách R&D ngay lập tức.15
|
Hạng mục Ưu tiên (WHO 2024) |
Chủng Vi khuẩn Đáng chú ý |
Đặc điểm Kháng thuốc và Mức độ Đe dọa Toàn cầu |
|
Đặc biệt Khẩn cấp (Critical) |
Acinetobacter baumannii(CRAB) |
Kháng Carbapenem; tỷ lệ tử vong cực cao tại ICU; nguyên nhân hàng đầu gây nhiễm khuẩn huyết và VAP; khả năng lây lan nhanh qua môi trường bề mặt y tế. |
|
Đặc biệt Khẩn cấp (Critical) |
Enterobacteriaceae (bao gồm E. coli, K. pneumoniae) |
Kháng Carbapenem và/hoặc Cephalosporin thế hệ 3; cơ chế truyền gen kháng thuốc qua plasmid dễ dàng lây lan giữa các loài vi khuẩn. |
|
Đặc biệt Khẩn cấp (Critical) |
Mycobacterium tuberculosis |
Kháng Rifampicin; gánh nặng bệnh tật khổng lồ, đặc biệt đe dọa các chương trình kiểm soát bệnh lao toàn cầu tại các nước đang phát triển. |
|
Cao (High) |
Pseudomonas aeruginosa(CRPA) |
Kháng Carbapenem; gây nhiễm trùng cơ hội nghiêm trọng, đặc biệt nguy hiểm trên bệnh nhân bỏng, bệnh nhân xơ nang và suy giảm miễn dịch. |
|
Cao (High) |
Staphylococcus aureus(MRSA) |
Kháng Methicillin; mầm bệnh Gram dương cực kỳ phổ biến gây viêm nội tâm mạc, nhiễm trùng da, mô mềm và nhiễm khuẩn huyết. |
|
Cao (High) |
Enterococcus faecium (VRE) |
Kháng Vancomycin; khả năng tồn tại lâu dài trong môi trường ruột và bề mặt, thường gây nhiễm trùng liên quan đến ống thông tiểu và thiết bị y tế. |
Việc CRAB tiếp tục duy trì vị trí thống trị trong nhóm "Đặc biệt Khẩn cấp" từ năm 2017 đến 2024 phản ánh một xu hướng đáng lo ngại: tình trạng kháng lại các kháng sinh chiến lược tuyến cuối đang diễn biến tồi tệ hơn, trong khi việc khám phá và phê duyệt các dòng kháng sinh mới nhắm vào cấu trúc phức tạp của vi khuẩn Gram âm lại đang bị đình trệ.15 Sự vắng mặt của các giải pháp điều trị triệt để buộc các hệ thống y tế phải thay đổi mô hình tiếp cận. Báo cáo của WHO nhấn mạnh việc sử dụng danh sách này như một kim chỉ nam không chỉ cho các nhà phát triển thuốc, viện nghiên cứu, và đối tác công-tư đầu tư vào R&D, mà còn cho các nhà hoạch định chính sách y tế.15
Mặc dù khung phân tích của WHO vô cùng hiệu quả trong việc thiết lập ưu tiên y tế nhân loại, một số chuyên gia nghiên cứu cũng chỉ ra rằng phương pháp tiếp cận chủ yếu xoay quanh con người (human-centric) có thể chưa đánh giá đầy đủ các động lực thúc đẩy AMR từ hệ sinh thái rộng lớn hơn, như nông nghiệp và môi trường nước (One Health approach).16 Dẫu vậy, sự hiện diện của A. baumannii ở vị trí đỉnh bảng không để lại bất kỳ nghi ngờ nào về việc nó là mục tiêu số một cần phải theo dõi và triệt tiêu trong không gian bệnh viện. Báo cáo WHO 2024 là lời khẳng định đanh thép rằng, trước khi một loại siêu kháng sinh mới ra đời, phòng ngừa sự lây nhiễm thông qua chẩn đoán sớm và vệ sinh môi trường chính là vũ khí hiệu quả duy nhất mà nhân loại có trong tay.
Phân tích Dữ liệu Kháng thuốc từ ECDC (2022)
Sự chuyển dịch lý thuyết từ khung ưu tiên của WHO được cụ thể hóa bằng những con số thống kê khốc liệt thông qua báo cáo giám sát dịch tễ học của Trung tâm Phòng ngừa và Kiểm soát Dịch bệnh Châu Âu (ECDC) phối hợp cùng WHO Khu vực Châu Âu, xuất bản vào năm 2022. Các dữ liệu thu thập được từ mẫu phân lập xâm lấn của các bệnh nhân đã vẽ nên một bản đồ dịch tễ học phức tạp, phản ánh sự suy yếu của hệ thống phòng thủ y tế công cộng trên toàn lục địa già.
Theo ước tính tổng quát từ ECDC, mỗi năm khu vực Liên minh Châu Âu và Khu vực Kinh tế Châu Âu (EU/EEA) phải hứng chịu hơn 670.000 ca nhiễm trùng xuất phát từ vi khuẩn kháng thuốc.20 Hậu quả trực tiếp của các ca nhiễm trùng này là khoảng 33.000 sinh mạng bị tước đoạt mỗi năm.20 Để cung cấp một cái nhìn chi tiết, dữ liệu từ hai mạng lưới giám sát khổng lồ là Mạng lưới Giám sát Kháng Kháng sinh Châu Âu (EARS-Net) – thu thập dữ liệu từ 30 quốc gia thuộc EU/EEA, và Mạng lưới Giám sát Kháng Kháng sinh Trung Á và Châu Âu (CAESAR) – gồm 17 quốc gia, đã được tổng hợp và phân tích chuyên sâu.21
Một trong những phát hiện mang tính cấu trúc quan trọng nhất từ dữ liệu ECDC là sự tồn tại của một độ dốc dịch tễ học (epidemiological gradient) đặc trưng kéo dài từ Bắc xuống Nam và từ Tây sang Đông trên khắp Châu Âu.20 Các quốc gia ở phía Bắc và phía Tây Châu Âu (nơi có các chính sách quản lý sử dụng kháng sinh chặt chẽ và nguồn lực kiểm soát nhiễm khuẩn dồi dào) thường duy trì tỷ lệ đề kháng ở mức tương đối thấp.21 Ngược lại, tại các khu vực phía Nam và phía Đông Châu Âu, tỷ lệ kháng thuốc, đặc biệt là kháng cephalosporin thế hệ 3 và carbapenem ở K. pneumoniae và kháng carbapenem ở Acinetobacter spp., đã leo thang lên những mức độ cực kỳ báo động.20 Sự chênh lệch địa lý này giải thích tại sao các bệnh viện lớn ở khu vực Tây Âu (như Thụy Sĩ), vốn là các trung tâm y tế trung chuyển tiếp nhận bệnh nhân từ nhiều vùng dịch tễ khác nhau, luôn phải đối mặt với rủi ro du nhập các siêu vi khuẩn đa kháng từ bên ngoài, biến các đợt bùng phát nội viện thành một mối đe dọa thường trực.
Sự tàn phá của AMR trở nên đặc biệt nghiêm trọng khi được đặt trong bối cảnh các đơn vị chăm sóc tích cực (ICU), nơi tập trung những bệnh nhân có sinh mệnh mong manh nhất. Dữ liệu chuyên đề của ECDC năm 2022 chỉ ra rằng, trong số các bệnh nhân lưu trú tại ICU trên hai ngày, có tới 9,8% xuất hiện ít nhất một loại nhiễm khuẩn bệnh viện (HAI).10 Việc sử dụng các thiết bị y tế xâm lấn để duy trì sự sống lại chính là con đường đưa mầm bệnh vào cơ thể: 83% các đợt viêm phổi có liên quan trực tiếp đến đặt nội khí quản, 43% các ca nhiễm trùng máu (BSI) liên quan đến catheter tĩnh mạch, và 95% các ca nhiễm trùng đường tiết niệu (UTI) xuất phát từ ống thông tiểu.10
Trong môi trường ICU khốc liệt này, Acinetobacter baumannii đã thể hiện một mức độ kháng thuốc kinh hoàng. Báo cáo ECDC xác nhận rằng có tới 74% các chủng phân lập A. baumannii thu thập từ bệnh nhân ICU trong mạng lưới giám sát thể hiện sự kháng lại hoàn toàn nhóm kháng sinh carbapenem.10 Để so sánh, tỷ lệ kháng carbapenem ở P. aeruginosa là 23% và ở Klebsiella spp. là 14%.10 Con số 74% này đồng nghĩa với việc đối với ba phần tư số bệnh nhân nhiễm A. baumannii tại ICU, phác đồ điều trị tiêu chuẩn bằng carbapenem hoàn toàn vô tác dụng, đẩy họ vào ranh giới sinh tử vô cùng mong manh.
|
Chỉ số Dịch tễ học tại ICU (Dữ liệu ECDC 2022) |
Tỷ lệ Phân bố và Kháng thuốc |
Ghi chú Phân tích Lâm sàng |
|
Tổng tỷ lệ mắc HAI (Lưu trú ICU > 2 ngày) |
9.8% |
Gần 1/10 bệnh nhân hồi sức cấp cứu bị lây nhiễm thêm mầm bệnh ngoại lai. |
|
Cấu trúc bệnh lý nhiễm khuẩn |
Viêm phổi: 6%; Nhiễm trùng máu (BSI): 4%; Nhiễm trùng tiểu (UTI): 3% |
Phản ánh sự rủi ro cực lớn của các can thiệp xâm lấn cơ học như máy thở và catheter. |
|
Kháng Carbapenem ở A. baumannii |
74% |
Mức kháng thuốc cao nhất trong tất cả các mầm bệnh Gram âm được giám sát, làm vô hiệu hóa phác đồ tuyến đầu. |
|
Kháng Carbapenem ở P. aeruginosa |
23% |
Đe dọa đáng kể nhưng vẫn thấp hơn rất nhiều so với phổ kháng của nhóm Acinetobacter. |
|
Kháng Carbapenem ở Klebsiella spp. |
14% |
Mặc dù tỷ lệ thấp hơn nhưng cơ chế lây lan qua plasmid khiến mầm bệnh này cực kỳ khó lường. |
Sự trỗi dậy của Acinetobacter trong khu vực EU/EEA không phải là một quá trình tịnh tiến tuyến tính, mà là một sự bùng nổ mang tính đột phá được ghi nhận thông qua biến động dữ liệu giữa các năm. Đặc biệt, từ năm 2020 đến 2021, số lượng các ca nhiễm khuẩn huyết do Acinetobacter spp. (phần lớn thuộc phức hợp A. baumannii) đã gia tăng một cách bất thường. Phân tích từ các phòng thí nghiệm tham gia báo cáo liên tục cho thấy mức tăng dao động từ 43% trên toàn mạng lưới cho đến 57% so với đường cơ sở của giai đoạn 2018-2019.23 ECDC đã đưa ra một kết luận chấn động: sự gia tăng quy mô lớn và có ý nghĩa thống kê này không phải là hệ quả của việc cải thiện kỹ thuật báo cáo hay mở rộng quy mô lấy mẫu.24 Thay vào đó, nó phản ánh một sự gián đoạn cấu trúc nghiêm trọng trong các hoạt động phòng ngừa và kiểm soát nhiễm khuẩn (IPC), một tác động trực tiếp và khốc liệt từ thảm họa y tế toàn cầu mang tên đại dịch COVID-19.23
Tác động Xúc tác của Đại dịch COVID-19 (Dữ liệu CDC 2022)
Nếu dữ liệu Châu Âu phác họa mức độ bùng phát diện rộng, thì Báo cáo Đặc biệt năm 2022 của Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (CDC) cung cấp lời giải thích cơ học chi tiết về cách thức đại dịch COVID-19 đã phá vỡ hoàn toàn thành trì phòng chống nhiễm khuẩn. Trong nhiều năm trước đại dịch, Kế hoạch Hành động Quốc gia Hoa Kỳ về Chống Vi khuẩn Kháng Kháng sinh (2020–2025) đã đạt được những tiến bộ mang tính bước ngoặt, liên tục làm giảm tỷ lệ lưu hành của các nhiễm khuẩn bệnh viện thông qua các can thiệp vệ sinh nghiêm ngặt tại các cơ sở chăm sóc sức khỏe.25 Tuy nhiên, COVID-19 đã tạo ra một "cơn bão hoàn hảo" vô tiền khoáng hậu, đảo ngược toàn bộ những thành tựu khó khăn mới đạt được này.
Dữ liệu năm 2022 của CDC tiết lộ một bức tranh tăm tối: ngay trong năm đầu tiên của đại dịch (từ năm 2019 đến năm 2020), tỷ lệ các bệnh nhiễm khuẩn bệnh viện (HAI) và số ca tử vong do các vi sinh vật đa kháng thuốc (MDRO) đã đồng loạt tăng 15%.26Phân tích dịch tễ học sâu hơn chỉ ra rằng, gần 40% số người mắc các bệnh nhiễm trùng kháng thuốc này đã bị lây nhiễm ngay trong thời gian họ đang được điều trị nội trú tại bệnh viện, một minh chứng rõ ràng cho sự thất bại của các quy trình cách ly vô trùng.27 Mặc dù hệ thống y tế đã phải vật lộn với những khoảng trống dữ liệu khổng lồ do sự chậm trễ trong khâu phát hiện và báo cáo trong thời kỳ đại dịch, những ước tính từ dữ liệu cơ sở năm 2019 vẫn cho thấy gánh nặng trước đại dịch đã là một thảm họa: ít nhất 2,8 triệu ca nhiễm trùng kháng thuốc xảy ra hàng năm tại Mỹ, cướp đi sinh mạng của hơn 35.000 người.27
Sự gián đoạn do đại dịch không tác động đồng đều lên tất cả các mầm bệnh. Khi phân tích sự gia tăng của từng tác nhân cụ thể, biểu đồ sinh thái của các vi sinh vật tại ICU đã có sự dịch chuyển kinh hoàng. Nhiễm trùng nấm Candida auris kháng thuốc tăng 60%; Enterobacterales kháng carbapenem (CRE) tăng 35%; và Pseudomonas aeruginosa đa kháng tăng 32%.26 Tuy nhiên, vượt lên trên tất cả các chỉ số này, tỷ lệ lây nhiễm của Acinetobacter kháng carbapenem (CRAB) đã bùng nổ với mức tăng phi mã và gây sốc nhất: 78%.25
|
Vi sinh vật Đa kháng thuốc (MDRO) Cảnh báo |
Mức tăng trưởng đột biến (2019 - 2020) theo CDC |
Phân tích Tác động và Cơ chế Lây nhiễm Nội viện |
|
Acinetobacter kháng Carbapenem (CRAB) |
+78% |
Phản ánh sự lây nhiễm chéo nghiêm trọng qua môi trường bề mặt, thiết bị thở máy và sự tồn tại dai dẳng của màng sinh học. |
|
Nấm Candida auris kháng thuốc |
+60% |
Tăng cường lây lan do khả năng bám dính lâu dài trên da bệnh nhân và bề mặt phòng bệnh trong bối cảnh thiếu hụt vật tư làm sạch. |
|
Enterobacterales kháng Carbapenem (CRE) |
+35% |
Liên quan mật thiết đến sự suy giảm miễn dịch chung và xu hướng sử dụng kháng sinh kinh nghiệm phổ rộng quá mức để chống lại bội nhiễm. |
|
Enterobacterales sinh ESBL |
+32% |
Lây lan nhanh qua đường tiếp xúc tay và các thiết bị chăm sóc cá nhân không được khử khuẩn triệt để. |
|
Pseudomonas aeruginosa Đa kháng (MDR) |
+32% |
Tấn công mạnh mẽ vào hệ thống hô hấp vốn đã bị tàn phá nặng nề bởi virus SARS-CoV-2 và tổn thương cơ học do máy thở. |
|
Enterococcus kháng Vancomycin (VRE) |
+14% |
Sự suy giảm tần suất vệ sinh bề mặt làm tăng tỷ lệ lây nhiễm mầm bệnh đường ruột qua đường tiếp xúc trực tiếp. |
Mức tăng vọt 78% của CRAB là hệ quả trực tiếp của sự cộng hưởng từ nhiều rào cản mang tính cấu trúc trong thời kỳ đại dịch. Thứ nhất, dòng bệnh nhân mắc COVID-19 hô hấp cấp ồ ạt tràn vào các đơn vị hồi sức đã vắt kiệt công suất vật lý và nhân lực của hệ thống y tế, làm quá tải các phòng cách ly áp lực âm.29 Thứ hai, sự thiếu hụt nghiêm trọng trong chuỗi cung ứng toàn cầu về thiết bị bảo hộ cá nhân (PPE) buộc các nhân viên y tế phải tái sử dụng áo choàng và găng tay khi di chuyển giữa các bệnh nhân, vô tình biến họ thành các vector cơ học khuếch tán vi khuẩn.29 Thứ ba, các bệnh nhân COVID-19 nguy kịch buộc phải duy trì tình trạng thở máy kéo dài trong nhiều tuần, tạo ra một khoang lưu trú nhân tạo hoàn hảo cho A. baumannii bám rễ, nhân lên và xả mầm bệnh vào phổi cũng như ra ngoài không khí phòng bệnh. Cuối cùng, việc chuyển hướng các nguồn lực phòng xét nghiệm sang xét nghiệm PCR tìm virus SARS-CoV-2 đã làm chậm trễ trầm trọng năng lực nuôi cấy và định danh vi khuẩn kháng thuốc. Sự chậm trễ trong dữ liệu dẫn đến sự chậm trễ trong hành động cách ly, cho phép vi khuẩn tự do lây lan trước khi các biện pháp phòng ngừa giọt bắn và tiếp xúc kịp thời được thiết lập.29
Hậu quả của sự gián đoạn này không dừng lại khi làn sóng COVID-19 đi qua. Các cập nhật dữ liệu mới nhất của CDC trong các năm 2021 và 2022 cho thấy sáu loại vi khuẩn kháng thuốc gây nhiễm khuẩn bệnh viện có tỷ lệ gia tăng kết hợp lên tới 20% so với thời kỳ tiền đại dịch. Đỉnh điểm là vào năm 2021 và duy trì ở mức cao nguy hiểm xuyên suốt năm 2022.28 Đặc biệt, số lượng các ca nhiễm C. auris trên lâm sàng đã tăng gấp 5 lần từ năm 2019 đến 2022, minh chứng cho việc khi hệ thống kiểm soát vệ sinh bị chọc thủng, các vi sinh vật cứng đầu sẽ tận dụng cơ hội định cư vĩnh viễn trong cơ sở hạ tầng bệnh viện.28 Cảnh báo của CDC vô cùng rõ ràng: sự tiếp diễn của xu hướng lây lan này sẽ kích hoạt một sự gia tốc tiến hóa, thúc đẩy sự xuất hiện của các chủng vi khuẩn kháng thuốc diện rộng (XDR) và vi khuẩn toàn kháng (pan-drug resistant).25 Nếu điều này xảy ra, nền tảng của y học can thiệp hiện đại sẽ bị phá hủy, đưa nhân loại quay ngược trở lại thời kỳ tăm tối của kỷ nguyên tiền kháng sinh.
Nút thắt Chẩn đoán và Bước đột phá của Môi trường Nuôi cấy Sinh màu (CHROMagar™)
Sự sụp đổ của các quy trình kiểm soát nhiễm khuẩn trong đại dịch và các bi kịch rải rác như ca tử vong tại Thụy Sĩ đều quy tụ về một điểm yếu mang tính cấu trúc của hệ thống y tế: nút thắt trong khâu chẩn đoán vi sinh. Tại phần lớn các bệnh viện, quy trình phát hiện Acinetobacter vẫn phụ thuộc vào các phương pháp nuôi cấy vi sinh truyền thống sử dụng thạch máu cừu (SBA), thạch MacConkey, hoặc canh thang truyền tim não (BHI broth).13 Mặc dù các phương pháp này đã phục vụ y học trong suốt thế kỷ 20, nhưng chúng tồn tại một nhược điểm chí mạng: thời gian. Một quy trình nuôi cấy, phân lập khuẩn lạc, và kiểm tra tính nhạy cảm kháng sinh (AST) tiêu chuẩn thường đòi hỏi từ 48 đến 72 giờ.30 Hơn thế nữa, đối với các mẫu phẩm phức tạp như phết trực tràng hoặc mẫu môi trường, sự phát triển của vi khuẩn mục tiêu thường bị lấn át hoàn toàn bởi sự phát triển quá mức của hệ vi khuẩn chí (background flora), dẫn đến tỷ lệ âm tính giả rất cao hoặc buộc phải cấy chuyền nhiều lần.13 Khoảng thời gian 72 giờ này tạo ra một "khoảng trống dịch tễ" chết người, cho phép vi khuẩn tự do bám vào cơ thể nhân viên y tế và thiết bị y khoa, kịp thời lây nhiễm cho nhiều bệnh nhân khác trước khi kết quả kháng sinh đồ được trả về.
Khái niệm "Giám sát Chủ động" (Active Surveillance) ra đời để giải quyết bài toán này. Khác với chẩn đoán thụ động (chỉ cấy máu hoặc dịch cơ thể khi bệnh nhân đã lên cơn sốt và có biểu hiện nhiễm trùng huyết), giám sát chủ động hướng tới việc lấy mẫu sàng lọc bệnh nhân ngay khi nhập viện hoặc định kỳ trong quá trình lưu trú tại ICU. Mục tiêu là để xác định tình trạng mang vi khuẩn không triệu chứng (colonization) tại đường ruột, khoang mũi, da, hoặc sự xâm chiếm của vi khuẩn trong môi trường bề mặt bệnh viện.8 Đối với nhiều loại vi khuẩn Gram âm, việc định cư thành công trong hệ tiêu hóa chính là tiền đề sống còn trước khi chúng tràn lên đường hô hấp và gây ra viêm phổi liên quan đến thở máy (VAP).11
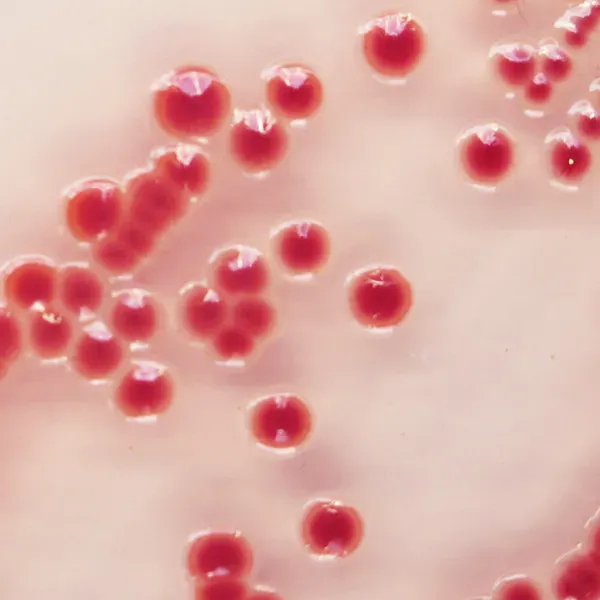
Công cụ định hình lại cuộc chơi trong lĩnh vực giám sát chủ động chính là công nghệ sinh màu (chromogenic media). Điển hình trong số đó là giải pháp Môi trường CHROMagar™ Acinetobacter, được phát triển dựa trên nền tảng công nghệ sinh màu tiên phong từ Paris.8 Môi trường này được thiết kế như một hệ thống kép: vừa chọn lọc (selective) vừa biệt hóa (differential).8Các tác nhân ức chế mạnh mẽ được tích hợp vào công thức thạch giúp tiêu diệt hầu hết các vi khuẩn Gram dương, nấm men (như C. albicans), cũng như ức chế các chủng trực khuẩn Gram âm không mang gen kháng carbapenem.8 Điều làm nên sự khác biệt cốt lõi là sự hiện diện của các cơ chất sinh màu độc quyền. Khi hệ men chuyển hóa đặc hiệu của A. baumannii tương tác với các cơ chất này trong quá trình phân giải chất dinh dưỡng, các khuẩn lạc sẽ nhanh chóng chuyển sang một màu sắc đặc trưng, thường là màu đỏ hoặc màu xanh mòng két (teal), có thể dễ dàng nhận diện bằng mắt thường.13
Tốc độ là lợi thế tuyệt đối của CHROMagar™. Quá trình hiển thị màu sắc và tạo khuẩn lạc hoàn tất chỉ sau 18 đến 24 giờ ủ trong môi trường hiếu khí ở 35-37°C.8 Các nghiên cứu đánh giá lâm sàng độc lập đã chứng minh rằng khi tiến hành phết mẫu trực tràng để phát hiện sự mang trùng của A. baumannii đa kháng (MDRAB) ở những bệnh nhân nguy kịch, CHROMagar™ đạt độ nhạy lên tới 91,7% và độ đặc hiệu đạt 89,6% so với tiêu chuẩn vàng là xét nghiệm sinh học phân tử PCR.11 Nhờ vậy, môi trường sinh màu này cho phép sàng lọc quy mô lớn trên các mẫu phết phân, mũi, vết thương, nước tiểu và đặc biệt là mẫu môi trường với độ chính xác và tốc độ vượt trội.8 Mặc dù CHROMagar™ không nhằm mục đích thay thế hoàn toàn cho các quy trình chẩn đoán khẳng định bệnh lý nhiễm trùng, nó đóng vai trò tối quan trọng như một hệ thống "cảnh báo sớm" vô giá.8 Nó trao cho các nhà quản lý nhiễm khuẩn quyền năng nhận diện và cô lập các ổ dịch tiềm tàng chỉ trong vòng chưa đầy 24 giờ, biến việc theo dõi thời gian thực sự tồn tại của MDRAB trở thành một thực tế có thể khả thi trên lâm sàng.
Chiến dịch Xóa sổ Kháng thuốc Ngoạn mục tại Chapel Hill (2008)
Hiệu quả lý thuyết của việc kết hợp giám sát chủ động và công nghệ sinh màu đã được minh chứng bằng một trong những chiến dịch kiểm soát nhiễm khuẩn xuất sắc nhất trong y văn cận đại. Trái ngược hoàn toàn với sự kiện bế tắc và tổn thất sinh mạng tại Thụy Sĩ, nhóm chuyên gia tại Bệnh viện thuộc Đại học North Carolina (UNC) ở Chapel Hill (Hoa Kỳ) đã thể hiện một năng lực kiểm soát rủi ro sinh học ở mức độ bậc thầy trong đợt bùng phát A. baumannii năm 2008.
Trung tâm điều trị bỏng của UNC Chapel Hill là một đơn vị chăm sóc tích cực khu vực gồm 15 giường bệnh, chuyên tiếp nhận các ca chấn thương nhiệt phức tạp với hệ miễn dịch suy kiệt.7 Sóng gió ập đến khi hệ thống theo dõi lâm sàng ghi nhận 9 bệnh nhân đồng loạt xuất hiện các biến chứng nhiễm trùng liên quan đến A. baumannii. Phân tích bệnh án cho thấy cấu trúc bệnh lý cực kỳ điển hình của các đợt bùng phát nội viện: ba ca bệnh viêm phổi mắc phải tại bệnh viện (HAP), bốn ca nhiễm trùng da/mô mềm tại vị trí ghép da, và hai ca nhiễm trùng đường tiết niệu.7 Toàn bộ 9 trường hợp này đều khởi phát các triệu chứng rõ rệt sau khi bệnh nhân đã lưu trú tại đơn vị bỏng vượt quá 48 giờ, xác nhận chắc chắn đây là một vụ lây nhiễm chéo nội viện (nosocomial outbreak).7
Đứng trước nguy cơ dịch bệnh lan rộng có thể quét sạch tính mạng của các bệnh nhân đang giành giật sự sống, nhóm chuyên gia tại Phòng Xét nghiệm Vi sinh Lâm sàng và Miễn dịch học do Tiến sĩ Peter Gilligan dẫn đầu đã từ chối quy trình nuôi cấy mất thời gian truyền thống.13 Thay vào đó, họ nhanh chóng triển khai một chiến dịch giám sát chủ động toàn diện, đánh giá và ứng dụng song song giải pháp canh thang BHI bổ sung Imipenem truyền thống và môi trường CHROMagar™ Acinetobacter.13 Hàng trăm mẫu phết bề mặt môi trường và mẫu đường hô hấp (258 mẫu bề mặt, 257 mẫu hô hấp) đã được thu thập liên tục từ các bệnh nhân nội trú trong khoảng thời gian từ tháng 7 đến tháng 11 năm 2008.13
Hiệu suất của công nghệ sinh màu đã tỏa sáng rực rỡ. Khi đọc kết quả chỉ sau 24 giờ ủ, những khuẩn lạc màu xanh mòng két (teal) báo hiệu sự hiện diện của Acinetobacter đã xuất hiện rõ nét trên các đĩa thạch CHROMagar™.13 Khi kiểm chứng lại bằng máy tự động Vitek2 và phương pháp khuếch tán đĩa kháng sinh đồ, kết quả xác nhận CHROMagar™ đã phân lập thành công 30 trên tổng số 31 chủng MDR Acinetobacter, tương đương với tỷ lệ phát hiện gần như tuyệt đối, đồng thời loại bỏ được sự sai lệch do các vi khuẩn không kháng thuốc gây ra.13 Khả năng cung cấp bản đồ phân bố mầm bệnh với tốc độ chớp nhoáng của CHROMagar™ đã định hướng cho các nhà dịch tễ học rà soát môi trường vô trùng một cách có chủ đích.
Kết quả của cuộc truy vết vi sinh đã phơi bày một nguồn lây nhiễm cực kỳ bất ngờ, vượt ra ngoài các phác đồ kiểm soát vệ sinh bề mặt thông thường. Bằng cách phết mẫu trên các thiết bị, nhóm nghiên cứu phát hiện ra rằng hai chiếc quạt bàn (table fans) được sử dụng để làm mát và lưu thông không khí cục bộ cho bệnh nhân chính là "ổ chứa" của siêu vi khuẩn.7 Phân tích kháng sinh đồ chứng minh rằng vi khuẩn MDR A. baumannii phân lập từ các lồng quạt bàn có phổ kháng thuốc giống hệt 100% với các chủng phân lập từ các bệnh nhân bị nhiễm trùng máu và viêm phổi.7 Do thiếu các hướng dẫn cụ thể từ Ủy ban Liên thẩm định (Joint Commission) về việc cấm sử dụng quạt trong không gian bệnh viện, các thiết bị cơ học vô hại này đã vô tình trở thành hệ thống khuếch tán khí dung (aerosolization), thổi màng sinh học chứa hàng triệu vi khuẩn A. baumannii vào không khí, gieo rắc trực tiếp lên da hở và hệ hô hấp của các bệnh nhân bỏng trong phòng.7 Khám phá này mang tính quyết định, bởi ngoài quạt bàn, không có bất kỳ mẫu bề mặt nào khác trong phòng cho kết quả dương tính, chứng tỏ vector lây truyền đã được "bắt tại trận".7
Hành động can thiệp ngay sau đó mang tính dứt khoát và toàn diện. Bệnh viện lập tức ban hành và thực thi một chính sách quản lý quạt nghiêm ngặt chưa từng có, cấm hoặc quản lý chặt chẽ sự luân chuyển thiết bị tạo gió trong môi trường ICU.7 Kết hợp với giao thức làm sạch triệt để (terminal cleaning) được tiến hành trên toàn bộ cấu trúc không gian phòng bệnh nhằm tiêu diệt màng sinh học tồn dư, chuỗi lây truyền đã bị bẻ gãy một cách tuyệt đối.7
Thành quả của chiến dịch can thiệp có sự trợ lực của CHROMagar™ là một phép màu về mặt dịch tễ: sự bùng phát đã được dập tắt hoàn toàn. Dữ liệu giám sát hồi cứu cho thấy, các chủng A. baumannii đa kháng thuốc đã bị loại bỏ một cách triệt để khỏi trung tâm bỏng này. Trong suốt chu kỳ hai năm theo dõi tiếp theo, bệnh viện duy trì được trạng thái sạch bóng MDRAB, với chỉ vỏn vẹn hai ca nhiễm A. baumannii ngoại lai, rời rạc và không có tính chất lây lan nội viện được ghi nhận mỗi năm.7 Chiến thắng tại Chapel Hill là minh chứng vĩ đại nhất cho sức mạnh của sự kết hợp giữa tư duy giám sát chủ động thời gian thực và sự linh hoạt trong quyết định lâm sàng, khẳng định rằng ngay cả những ổ dịch kháng thuốc tàn khốc nhất cũng có thể bị tiêu diệt hoàn toàn nếu thời gian chẩn đoán được rút ngắn đủ nhanh.
Kết luận và Đề xuất Khung Chiến lược Quản trị Rủi ro Sinh học
Sự song hành của hai câu chuyện lâm sàng – một bi kịch đau xót của nạn nhân vụ cháy rừng Crans-Montana tại Bệnh viện Đại học Zürich và một chiến dịch xóa sổ dịch bệnh rực rỡ tại Chapel Hill – đã bóc trần bản chất cốt lõi của cuộc chiến chống lại vi khuẩn kháng kháng sinh (AMR) trong thế kỷ 21. Sự thất bại tại Thụy Sĩ không phản ánh sự yếu kém của y học phẫu thuật hay kỹ thuật hồi sức, mà phản ánh một sự sụp đổ trong tư duy phòng ngự vi sinh. Khi y học hiện đại vẫn tập trung vào việc tìm kiếm các phương pháp điều trị sau khi bệnh nhân đã rơi vào vòng xoáy của sốc nhiễm khuẩn do Acinetobacter baumannii, cái giá phải trả luôn là tổn thất sinh mạng, kéo theo hệ lụy kinh tế khổng lồ cho hệ thống y tế công cộng.
Khung cảnh báo toàn cầu của Tổ chức Y tế Thế giới (WHO) năm 2024, đặt A. baumannii kháng carbapenem vào đỉnh kim tự tháp ưu tiên đặc biệt khẩn cấp, là một minh chứng không thể chối cãi về sự khan hiếm của các lựa chọn trị liệu bằng thuốc trong tương lai gần.15 Bức tranh dịch tễ học Châu Âu do ECDC công bố năm 2022, với tỷ lệ kháng carbapenem chạm ngưỡng 74% tại các ICU và độ dốc dịch tễ lan rộng từ Đông sang Tây, khẳng định rằng rủi ro lây nhiễm chéo không biên giới là một hiện tại tàn khốc.10 Sự tàn phá cấu trúc kiểm soát lây nhiễm trong thời kỳ đại dịch COVID-19, được CDC chứng minh qua sự gia tăng kinh hoàng 78% số ca mắc CRAB tại Hoa Kỳ, cho thấy lớp vỏ bọc an toàn của các bệnh viện mỏng manh đến mức nào trước sự cạn kiệt nguồn lực.26 Tuy nhiên, bài học lịch sử từ chiến dịch Chapel Hill (2008) chứng minh rằng xu hướng tăm tối này có thể bị bẻ gãy hoàn toàn. Bằng cách tái cấu trúc tư duy từ "chẩn đoán thụ động" sang "giám sát chủ động" với sự tham gia của các nền tảng sinh màu nhanh chóng như CHROMagar™ Acinetobacter, các nhà lâm sàng có thể đi trước vi khuẩn một bước.7
Hình 4. Giao thức kiểm soát nhiễm khuẩn cốt lõi nhằm ngăn chặn lây nhiễm chéo nội viện. Tổng hợp trực quan các can thiệp thực hành lâm sàng tiêu chuẩn, bao gồm tuân thủ vệ sinh tay, sử dụng trang phục bảo hộ cá nhân (PPE), khử trùng môi trường bề mặt nghiêm ngặt, thiết lập phòng cách ly chuyên biệt và quản lý sử dụng kháng sinh hợp lý.
Để bảo vệ không gian chăm sóc tích cực, một khung chiến lược quản trị rủi ro sinh học toàn diện cần được hiện thực hóa ở cả cấp độ chính sách và thực hành lâm sàng. Trước tiên, quy trình giám sát chủ động (Active Surveillance) cần được luật hóa để trở thành một tiêu chuẩn chăm sóc bắt buộc (standard of care) tại tất cả các ICU và trung tâm bỏng trên toàn cầu. Các bệnh nhân thuộc nhóm nguy cơ cao, có diện tích bỏng lớn hoặc suy giảm miễn dịch, phải được phết mẫu sàng lọc ngay tại thời điểm nhập viện và định kỳ mỗi tuần để xác định tình trạng mang vi khuẩn không triệu chứng. Việc áp dụng các loại môi trường sinh màu cho kết quả trong 24 giờ phải thay thế các quy trình nuôi cấy truyền thống trong các quyết định cách ly dịch tễ.
Thứ hai, việc kiểm toán vệ sinh môi trường không được giới hạn ở các bề mặt truyền thống mà phải bao trùm toàn bộ các vật thể cơ học và hệ thống đối lưu khí trong phòng bệnh (như quạt bàn, hệ thống điều hòa, và thành giường). Các quy trình làm sạch triệt để phải tập trung vào việc phá vỡ cấu trúc màng sinh học polymer ngoại bào, kết hợp với các đợt kiểm tra vi sinh đột xuất. Cuối cùng, việc đầu tư mạnh mẽ vào năng lực phòng xét nghiệm vi sinh lâm sàng là yếu tố then chốt. Sự thành công của Chapel Hill khẳng định rằng chi phí đầu tư cho hệ thống chẩn đoán sớm vô cùng nhỏ nhoi so với chi phí tổn thất do số ngày nằm viện kéo dài và tử vong do nhiễm khuẩn huyết. Việc liên tục theo dõi, phát hiện sớm và cách ly tuyệt đối vi khuẩn Acinetobacter baumanniikhông đơn thuần là một chỉ tiêu kỹ thuật y tế, mà chính là lớp rào chắn sinh tồn cuối cùng bảo vệ sự sống cho những sinh mệnh mỏng manh nhất trong hệ thống hồi sức cấp cứu.
Nguồn trích dẫn
- Crans-Montana: Brandopfer war im Unispital mit Krankenhauskeim infiziert - Watson, truy cập vào tháng 2 25, 2026, https://www.watson.ch/schweiz/wallis/548127707-crans-montana-brandopfer-war-im-unispital-mit-krankenhauskeim-infiziert
- 5900 Tote jährlich: Wie hoch ist das Risiko von Spitalkeimen? - Blick, truy cập vào tháng 2 25, 2026, https://www.blick.ch/schweiz/nach-tod-von-crans-montana-brandopfer-im-unispital-zuerich-wie-gross-ist-das-risiko-einer-spitalinfektion-id21656786.html
- Crans-Montana-Opfer stirbt an Spitalkeim: Bundesrat kannte Risiko | Beobachter, truy cập vào tháng 2 25, 2026, https://www.beobachter.ch/gesundheit/todliche-spitalkeime-der-bundesrat-ignoriert-die-gefahr-seit-jahren-904945
- Zwei Brandopfer von Crans-Montana fangen Spitalkeim ein - Nau.ch, truy cập vào tháng 2 25, 2026, https://www.nau.ch/news/schweiz/zwei-brandopfer-von-crans-montana-fangen-spitalkeim-ein-67090067
- Clinical infection in burn patients and its consequences - PubMed, truy cập vào tháng 2 25, 2026, https://pubmed.ncbi.nlm.nih.gov/29115647/
- Microbial infections in burn patients - ACC : Acute and Critical Care, truy cập vào tháng 2 25, 2026, https://www.accjournal.org/journal/view.php?number=1531
- Investigation of Acinetobacter baumannii Outbreak in a Burn Unit Revealed a Surprising Environmental Source - PMC, truy cập vào tháng 2 25, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10476506/
- CHROMagar™ Acinetobacter – Chromagar, truy cập vào tháng 2 25, 2026, https://www.chromagar.com/en/product/chromagar-acinetobacter/
- Outcomes of Acinetobacter baumannii infection in critically ill burned patients - PubMed, truy cập vào tháng 2 25, 2026, https://pubmed.ncbi.nlm.nih.gov/17351441/
- Healthcare-associated infections acquired in intensive care units - Annual Epidemiological Report for 2022 - ECDC, truy cập vào tháng 2 25, 2026, https://www.ecdc.europa.eu/en/publications-data/healthcare-associated-infections-acquired-intensive-care-units-annual-1
- Evaluation of CHROMagar Acinetobacter for Detection of Enteric Carriage of Multidrug-Resistant Acinetobacter baumannii in Samples from Critically Ill Patients - PMC, truy cập vào tháng 2 25, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC2708470/
- Variations of CHROMagar Acinetobacter to detect imipenem-resistant Acinetobacter baumannii – calcoaceticus complex, truy cập vào tháng 2 25, 2026, https://www.chromagar.com/wp-content/uploads/2021/10/1546421287Variations_of_CHROMagar_Acinetobacter_to_detect_imipenem_resistant_Acinetobacter_baumannii_calcoaceticus_complex.pdf
- CHROMagar Acinetobacter, truy cập vào tháng 2 25, 2026, https://www.chromagar.com/wp-content/uploads/2021/10/1299661636Poster_AC_Gilligan_09.pdf
- An Evaluation of Burn Infections Caused by Multidrug Resistant A.baumannii and the Treatment Approach - Journal of Current Surgery, truy cập vào tháng 2 25, 2026,https://www.currentsurgery.org/index.php/jcs/article/view/11/4
- WHO bacterial priority pathogens list, 2024: Bacterial pathogens of public health importance to guide research, development and strategies to prevent and control antimicrobial resistance, truy cập vào tháng 2 25, 2026, https://www.who.int/publications/i/item/9789240093461
- The 2024 WHO bacterial priority pathogens list: a critical evolution from a global One Health perspective - PMC, truy cập vào tháng 2 25, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC12830135/
- WHO* updates its priority bacterial pathogens list for 2024, to curb the spread of antimicrobial resistance, truy cập vào tháng 2 25, 2026, https://www.bmxclinicaldiagnostics-divil.com/post/who-pathogens-list2024
- WHO global priority pathogens list of antibiotic-resistant bacteria - Doherty Institute, truy cập vào tháng 2 25, 2026, https://www.doherty.edu.au/articles/who-global-priority-pathogens-list-of-antibiotic-resistant-bacteria/
- The WHO Bacterial Priority Pathogens List 2024: a prioritisation study to guide research, development, and public health strateg - Carb-X, truy cập vào tháng 2 25, 2026, https://carb-x.org/wp-content/uploads/2025/08/PIIS1473309925001185.pdf
- Antimicrobial resistance surveillance in Europe, 2022 - 2020 data - ECDC, truy cập vào tháng 2 25, 2026, https://www.ecdc.europa.eu/sites/default/files/documents/Joint-WHO-ECDC-AMR-report-2022.pdf
- Surveillance of antimicrobial resistance in Europe, 2022 data - ECDC, truy cập vào tháng 2 25, 2026, https://www.ecdc.europa.eu/sites/default/files/documents/Nov2023-ECDC-WHO-Executive-Summary.pdf
- Surveillance of antimicrobial resistance in Europe, 2021 data - Executive summary - ECDC, truy cập vào tháng 2 25, 2026, https://www.ecdc.europa.eu/sites/default/files/documents/Nov2022-ECDC-WHO-Executive-Summary_Final%20with%20identifiers.pdf
- Large increase in bloodstream infections with carbapenem-resistant Acinetobacter species during the first 2 years of the COVID-19 pandemic, EU/EEA, 2020 and 2021 - PMC, truy cập vào tháng 2 25, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC9673235/
- Antimicrobial resistance in the EU/EEA (EARS-Net) AER for 2021 - ECDC, truy cập vào tháng 2 25, 2026, https://www.ecdc.europa.eu/sites/default/files/documents/AER-EARS-Net-2021_2022-final.pdf
- The pandemic legacy of antimicrobial resistance in the USA - PMC - NIH, truy cập vào tháng 2 25, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC9365317/
- CDC 2022 Special Report: COVID-19 U.S. Impact on Antimicrobial Resistance, truy cập vào tháng 2 25, 2026, https://www.biomerieux.com/us/en/education/resource-hub/solution-education/antimicrobial-resistance/cdc-2022-special-report-covid-19-us-impact-on-antimicrobial-resistance.html
- COVID-19 & Antimicrobial Resistance - CDC, truy cập vào tháng 2 25, 2026, https://www.cdc.gov/antimicrobial-resistance/data-research/threats/COVID-19.html
- Antimicrobial Resistance Threats in the United States, 2021-2022 - CDC, truy cập vào tháng 2 25, 2026, https://www.cdc.gov/antimicrobial-resistance/data-research/threats/update-2022.html
- 2022 SPECIAL REPORT: COVID-19 U.S. Impact on Antimicrobial Resistance - CDC, truy cập vào tháng 2 25, 2026, https://www.cdc.gov/antimicrobial-resistance/media/pdfs/covid19-impact-report-508.pdf
- Culture Media for Detection of Acinetobacter baumannii - Chromagar, truy cập vào tháng 2 25, 2026, https://www.chromagar.com/wp-content/uploads/2021/10/1471011710Acinetobacter.pdf
- (PDF) Co‐localization of clinically relevant antibiotic‐ and heavy metal resistance genes on plasmids in Klebsiella pneumoniae from marine bivalves - ResearchGate, truy cập vào tháng 2 25, 2026, https://www.researchgate.net/publication/372472291_Co-localization_of_clinically_relevant_antibiotic-_and_heavy_metal_resistance_genes_on_plasmids_in_Klebsiella_pneumoniae_from_marine_bivalves
- Modified CHROMagar Acinetobacter medium for direct detection of multidrug-resistant Acinetobacter strains in nasal and rectal swab samples - PubMed, truy cập vào tháng 2 25, 2026, https://pubmed.ncbi.nlm.nih.gov/23667846
- FINAL PROGRAM - ResearchGate, truy cập vào tháng 2 25, 2026, https://www.researchgate.net/profile/Nicodemus_M_Useh/publication/320961771_Inactivation_of_phoP_Gene_in_Clostridium_difficile_Affects_Cell_Fitness_and_Delays_Sporulation/links/5a04bf7e0f7e9bc4078f1585/Inactivation-of-phoP-Gene-in-Clostridium-difficile-Affects-Cell-Fitness-and-Delays-Sporulation.pdf
- (PDF) Cost Savings Incurred by Implementation of Routine Microbiological Identification by Matrix-Assisted Laser Desorption/Ionization-Time of Flight (MALDI-TOF) Mass Spectrometry - ResearchGate, truy cập vào tháng 2 25, 2026, https://www.researchgate.net/publication/277080277_Cost_Savings_Incurred_by_Implementation_of_Routine_Microbiological_Identification_by_Matrix-Assisted_Laser_DesorptionIonization-Time_of_Flight_MALDI-TOF_Mass_Spectrometry
- Synergistic mechanism of modified nZVI and Citrobacter reshaping sludge microbiome drives co-removal of HBCD and nutrients in municipal wastewater | Request PDF - ResearchGate, truy cập vào tháng 2 25, 2026, https://www.researchgate.net/publication/391551615_Synergistic_mechanism_of_modified_nZVI_and_Citrobacter_reshaping_sludge_microbiome_drives_co-removal_of_HBCD_and_nutrients_in_municipal_wastewater
- Assessment of Anaerobic Digestate of Dairy Manure as Biofertilizer: Environmental Risk and Potential in Suppressing Plant Diseas, truy cập vào tháng 2 25, 2026, https://obihiro.repo.nii.ac.jp/record/4349/files/Dissertation%28PanZhifei%29.pdf

CÔNG TY TNHH KHOA HỌC KỸ THUẬT TOÀN CẦU
Trụ sở: Lầu 19, khu A, số 4 Nguyễn Đình Chiểu, Phường Đa Kao, Quận 1, TP. Hồ Chí Minh, Việt Nam
VP HCM: 48 Châu Thị Hóa, Phường 4, Quận 8, TP. Hồ Chí Minh
VP HN: Số nhà 59B ngõ 148 Trần Duy Hưng, phường Trung Hòa, Quận Cầu Giấy, Hà Nội
Hotline: 0908.090.555
Email: dinh@global.net.vn
Website: https://globallab.com.vn/


Xem thêm