Thực hiện các nghiên cứu biểu hiện gen đơn mồi (singleplex) hoặc đa mồi (multiplex) và các xét nghiệm chẩn đoán một cách tin cậy với bộ kit mẫu dò mạnh mẽ, dẫn đầu thị trường này. Hỗn hợp mastermix tối ưu này cũng phù hợp cho nghiên cứu kiểu gen (genotyping) dựa trên qPCR và phân biệt alen (allelic discrimination). Hỗn hợp này cũng có sẵn phiên bản chứa thuốc nhuộm xanh giúp dễ dàng quan sát với tên gọi qPCRBIO Probe Blue Mix.
Đối với hầu hết các ứng dụng qPCR dùng mẫu dò, chúng tôi khuyên bạn nên dùng thử dòng Clara® Probe Mixes mới nhất của chúng tôi để có hiệu suất tốt nhất.
qPCRBIO Probe Mix là sự lựa chọn mạnh mẽ cho mọi nhu cầu Real-time PCR dùng mẫu dò của bạn. Bộ kit đa năng của chúng tôi có thể được sử dụng để phát hiện một cách tin cậy các mục tiêu có số lượng bản sao cực thấp và định lượng bất kỳ mẫu khuôn DNA nào, bao gồm trình tự gen (genomic DNA), cDNA và trình tự virus.
Đặc tính nổi bật
-
Hiệu suất cao trong các phản ứng đa mồi (multiplex).
-
Tốc độ kéo dài nhanh cho giá trị Ct sớm.
-
Độ nhạy dẫn đầu thị trường – tăng giới hạn phát hiện (LOD).
-
Khuếch đại hiệu quả từ các trình tự giàu GC và AT.
-
Công nghệ Hot-start ức chế bằng kháng thể.
-
Tương thích với tất cả các hệ thống máy Real-time PCR.
-
Có phiên bản mix màu xanh giúp dễ dàng quan sát.
Ứng dụng
-
Định lượng tuyệt đối.
-
Phân tích biểu hiện gen tương đối 2 bước (2-step RT-qPCR).
-
Mẫu dò TaqMan®, Scorpions® và Molecular Beacon.
-
Real-time PCR chẩn đoán.
-
Xác định kiểu gen (Genotyping) và phân biệt alen.
Bằng cách kết hợp công nghệ hot-start dựa trên kháng thể với những tiến bộ mới nhất trong hóa học hệ đệm, chúng tôi mang đến hiệu suất dẫn đầu thị trường mà không cần hoặc chỉ cần tối ưu hóa tối thiểu. Độ nhạy được tăng cường giúp qPCRBIO Probe Mix trở thành lựa chọn hoàn hảo cho chạy đa mồi (multiplexing).
qPCRBIO Probe Blue Mix chứa một loại thuốc nhuộm không gây phản ứng giúp tăng khả năng quan sát hỗn hợp, đặc biệt hữu ích trong việc giảm lỗi pipette khi nạp các phản ứng có thể tích nhỏ hoặc khi sử dụng đĩa PCR màu trắng.
Hãy sử dụng Công cụ Lựa chọn qPCR của chúng tôi để tìm biến thể ROX phù hợp với thiết bị của bạn.
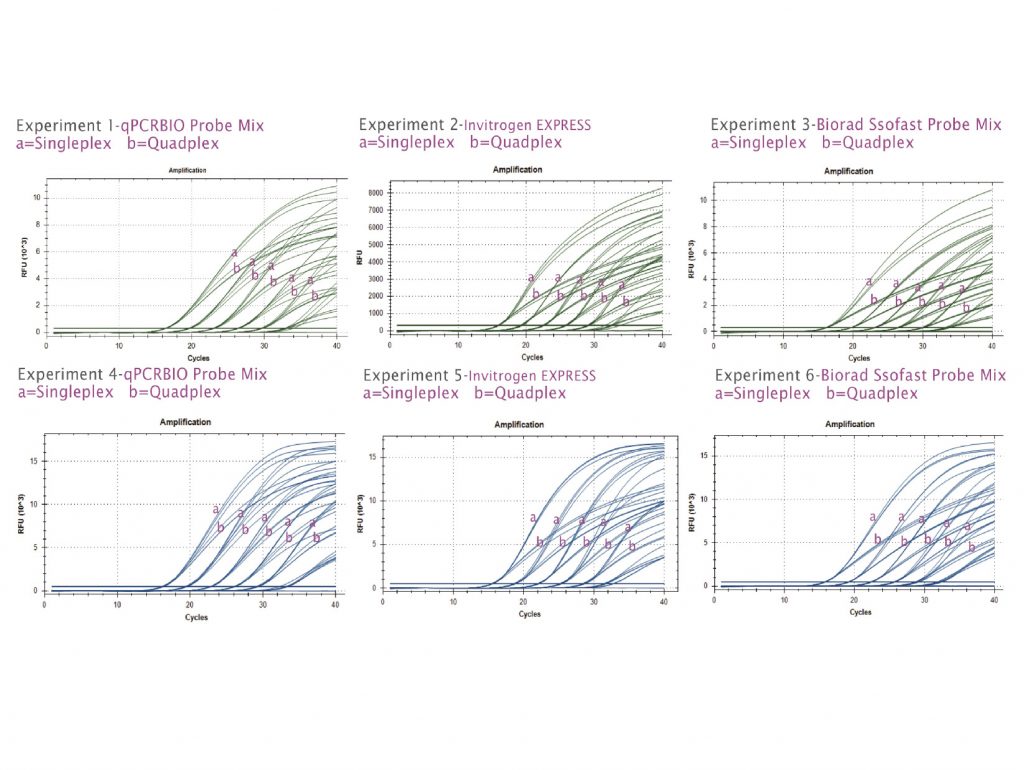
Thí nghiệm 1, 2 và 3: Cho thấy các đường tín hiệu khuếch đại mẫu dò TaqMan của gen ACVR2B người trong phản ứng đơn mồi và bốn mồi (quadplex: ACVR2B, LIMK1, ACVR1B và CDK7) từ một dãy pha loãng cDNA.
-
a) Các đường tín hiệu biểu thị phản ứng đơn mồi.
-
b) Các đường tín hiệu biểu thị phản ứng bốn mồi (quadplex). qPCRBIO Probe Mix đã được thử nghiệm đối chứng với các hỗn hợp mix mới nhất từ đối thủ Invitrogen (thí nghiệm 2) và Biorad (thí nghiệm 3). qPCRBIO Probe Mix cho thấy ít bị ức chế PCR nhất khi chạy đa mồi so với các hỗn hợp của Invitrogen và Biorad. Điều này được thể hiện rõ qua việc các đường tín hiệu khuếch đại trong phản ứng bốn mồi (b) ít bị trễ hơn so với phản ứng đơn mồi (a).
Thí nghiệm 4, 5 và 6: Cho thấy các đường tín hiệu khuếch đại mẫu dò TaqMan của gen LIMK1 người trong phản ứng đơn mồi và bốn mồi. Tương tự như các thí nghiệm trước, sự khuếch đại LIMK1 ít bị ức chế hơn trong phản ứng đa mồi khi dùng mix của PCR Biosystems so với các hỗn hợp đối thủ. Điều kiện chu trình nhiệt: 95°C trong 2 phút, 40 chu kỳ gồm 95°C trong 10 giây và 60°C trong 15 giây trên thiết bị Biorad CFX.
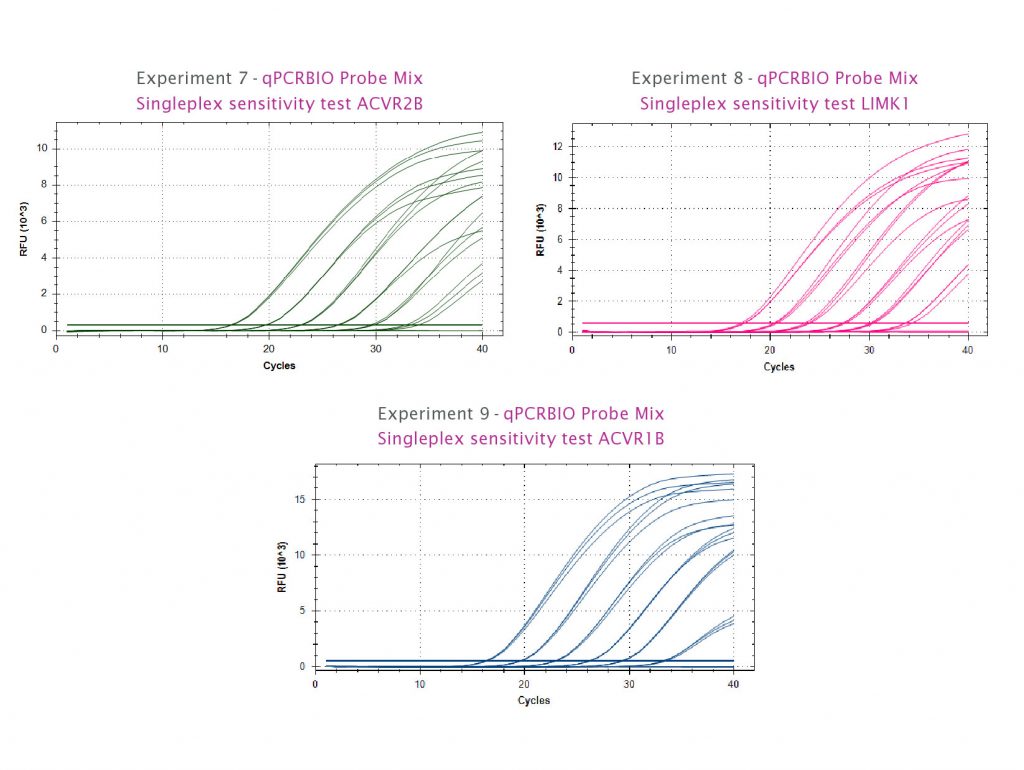
Thí nghiệm 7, 8 và 9: Cho thấy các đường tín hiệu khuếch đại mẫu dò TaqMan từ dãy pha loãng plasmid từ 1.000.000 bản sao xuống còn 10 bản sao DNA. Với mỗi gen, qPCRBIO Probe Mix đều khuếch đại với hiệu suất 100% và phát hiện được ở mức 10 bản sao DNA.
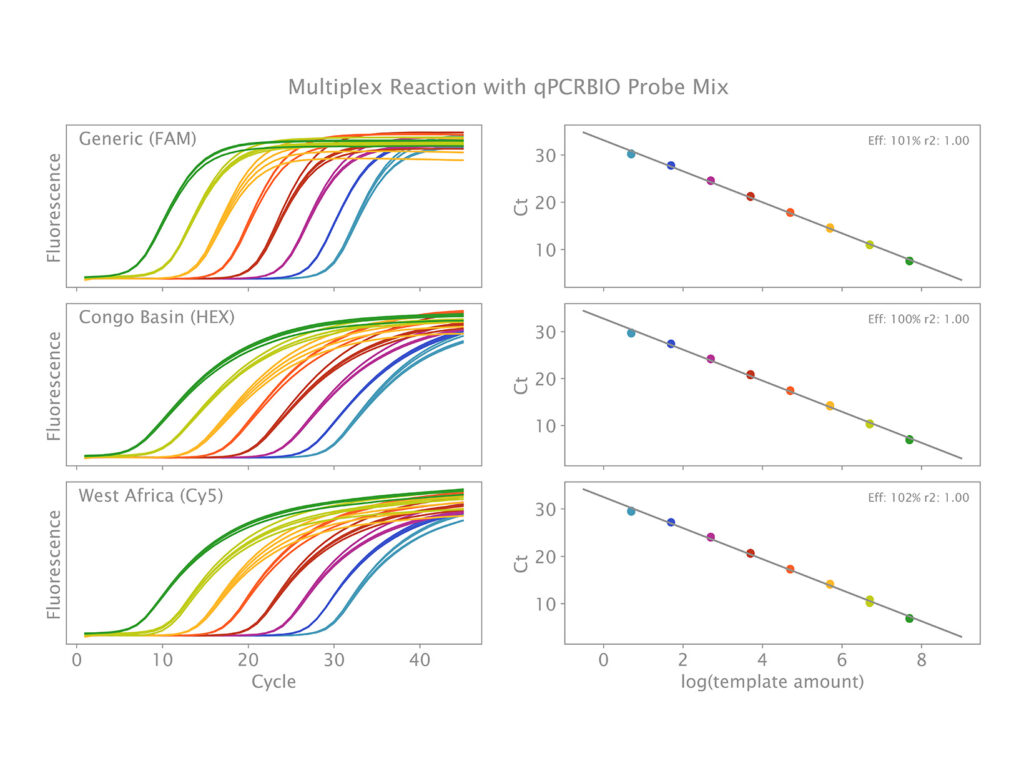
Phát hiện đa mồi hiệu quả và nhạy bén các mục tiêu DNA với qPCRBIO Probe Mix: Mẫu khuôn DNA của virus đậu mùa khỉ (MPOX) được chuẩn bị trong một dãy pha loãng 10 lần tại 8 điểm, dao động từ $5 \times 10^7$ đến 5 bản sao mỗi phản ứng. Phản ứng 3 mồi (3-plex) được thiết lập để phát hiện một mục tiêu MPOX chung và hai mục tiêu đặc hiệu cho các biến chủng lưu hành tại Lưu vực Congo và Tây Phi. Tất cả các nồng độ mục tiêu đều được phát hiện thành công trong dưới 30 chu kỳ với hiệu suất xấp xỉ 100%, cho thấy qPCRBIO Probe Mix hoàn toàn phù hợp để phát hiện mục tiêu nhạy và tin cậy ngay cả với các mẫu khuôn có nồng độ thấp
qPCRBIO Probe Mix Lo-RO
| Component |
100 Reactions |
500 Reactions |
2000 Reactions | 5000 Reactions | 5000 Reactions |
|
2x qPCRBIO Probe Mix Lo-ROX |
1 x 1mL | 5 x 1mL | 20 x 1mL | 1 x 50mL Bottle | 50 x 1mL in Pouch |
qPCRBIO Probe Mix Hi-ROX
| Component |
100 Reactions |
500 Reactions |
2000 Reactions | 5000 Reactions | 5000 Reactions |
| 2x qPCRBIO Probe Mix Hi-ROX | 1 x 1mL | 5 x 1mL | 20 x 1mL | 1 x 50mL Bottle | 50 x 1mL in Pouch |
qPCRBIO Probe Mix No-ROX
| Component |
100 Reactions |
500 Reactions |
2000 Reactions | 5000 Reactions | 5000 Reactions |
|
2x qPCRBIO Probe Mix No-ROX |
1 x 1mL | 5 x 1mL | 20 x 1mL | 1 x 50mL Bottle | 50 x 1mL in Pouch |
qPCRBIO Probe Mix Separate-ROX
| Component |
100 Reactions |
500 Reactions |
2000 Reactions | 5000 Reactions | 5000 Reactions |
| 2x qPCRBIO Probe Mix No-ROX | 1 x 1mL | 5 x 1mL | 20 x 1mL | 1 x 50mL Bottle | 50 x 1mL in Pouch |
| 50μM ROX Additive | 1 x 200μL | 1 x 200μL | 4 x 200μL | 2 x 520μL | 2 x 520μL |
| Reaction Volume | Storage |
| 20 μL | On arrival, products should be stored between -30 °C and -20 °C. If stored correctly the kit will retain full activity until the indicated expiry date. |
Instrument Compatibility
This product is compatible with all standard and fast cycling qPCR instruments. Use our qPCR Selection Tool to find out which ROX variant is compatible with your instrument.
Product Flyers
Product Manuals
PB20.21 qPCRBIO Probe Mix Lo-ROX Manual
PB20.22 qPCRBIO Probe Mix Hi-ROX Manual
PB20.23 qPCRBIO Probe Mix No-ROX Manual
PB20.24 qPCRBIO Probe Mix Separate-ROX Manual
PB20.25 qPCRBIO Probe Blue Mix Lo-ROX Manual
PB20.26 qPCRBIO Probe Blue Mix Hi-ROX Manual
PB20.27 qPCRBIO Probe Blue Mix Separate-ROX Manual
Material Safety Data Sheets
PB20.21 qPCRBIO Probe Mix Lo-ROX MSDS
PB20.22 qPCRBIO Probe Mix Hi-ROX MSDS
PB20.23 qPCRBIO Probe Mix No-ROX MSDS
PB20.24 qPCRBIO Probe Mix Separate-ROX MSDS
PB20.25 qPCRBIO Probe Blue Mix Lo-ROX MSDS
PB20.26 qPCRBIO Probe Blue Mix Hi-ROX MSDS
PB20.27 qPCRBIO Probe Blue Mix Separate-ROX MSDS
Certificate of Analysis Finder
ROX (6-carboxy-X-rhodamine) is used as a passive reference dye in ROX-dependent real-time PCR instruments to normalize for variations of fluorescence levels that can arise mainly due to optical path variations among wells. Normalisation of the fluorescence intensity (Rn) is done in real-time PCR software by dividing the emission intensity of the specific signal by the emission intensity of ROX.
ROX does not take part in the PCR reaction and its fluorescence levels are not proportional to the quantity of DNA in each well, so the addition of this fluorophore to a mix provides a constant fluorescent signal during amplification.
Different types of real-time PCR instruments requiring a passive reference standard have different optimal concentrations of ROX, mainly due to the different optical configurations of each system (i.e. the different type of excitation source and optics used).
The addition of either too little or too much ROX would result in a very noisy signal impacting on the results of the reaction. Therefore, it is extremely important for the user to:
- Determine the correct ROX concentration to optimise real-time PCR results, and
- Check the ROX settings on the software used to set up the reaction
A useful selection tool for the most commonly used systems can be found here.
qPCRBIO Probe Mixes are ready to use qPCR 2x Mastermixes. You only need to add primers, template DNA and PCR grade water during reaction set up.
ROX is a passive reference dye which means it does not take part in the PCR reaction. It is used to normalise non-PCR related fluctuations in fluorescence.
The qPCRBIO Probe Mixes that contain passive reference dyes come in different formulations, each with a different concentration of the passive reference dye:
- qPCRBIO Probe Mix Lo-ROX (PB20.21) contains 112 nM ROX.
- qPCRBIO Probe Mix Hi-ROX (PB20.22) contains 1.12 µM ROX.
- qPCRBIO Probe Mix No-ROX (PB20.23) does not contain ROX.
- qPCRBIO Probe Mix Separate-ROX (PB20.24) 2x mix contains no ROX and include a separate tube of 50 µM ROX additive. This enables you to choose what concentration of ROX you’d like to use.
You can use our qPCR Selection Tool under the Resources drop-down menu to determine which of our mixes are best suited for your qPCR machine.
Yes, PCR products generated with qPCRBIO Probe Mixes have the same characteristics as PCR products generated with wild-type Taq polymerase. They may be sequenced or digested with restriction endonucleases using standard protocols. Products are 3′-d(A)-tailed and may be used for TA cloning or may be blunt-ended or digested with restriction enzymes prior to cloning. For best results, we recommend purifying the PCR products using any standard PCR clean-up kit.
All qPCRBIO Probe Mixes contain MgCl2 at a concentration of 12 mM. This means the final concentration in the reaction is 6 mM.
All qPCRBIO Probe Mixes contain dNTPs at a concentration of 2 mM (0.5 mM each). This means the final concentration in the reaction is 1 mM (0.25 mM each).
Higher Ct values are generally indicative of delayed amplification. This could most likely be due to an excess of template in the reaction resulting in the primers and probes being bound on different DNA molecules. Samples usually have a lot of DNA other than the target gene and this can scatter the oligos. We recommend diluting the samples (10x-1000x) to solve this.
Moreover, annealing/extension temperature can also be increased to make the binding of the oligos more specific to the target sequence and decrease background signal.
It has been reported that efficiency can decrease with subsequent dilutions for the standard curve. We recommend avoiding this by diluting the standards in 10 mM Tris-HCl pH 8.0, 0.1 mM EDTA, 0.05% Tween-20. EDTA is a chelating agent and it plays a role in preventing DNAse activity1. Tween-20 is a detergent and prevents the DNA from adsorbing to the sides of the tubes2. Most microcentrifuges are made of polypropylene and research has demonstrated that DNA sticks very well to polypropylene3.
Standards should not be frozen after diluting them. Even in the presence of detergent, freezing seems to cause DNA to bind irreversibly to polypropylene. We suggest leaving your standards at 4°C and preparing a fresh batch every few weeks.
1 Barra, G. B. et al. EDTA-mediated inhibition of DNases protects circulating cell-free DNA from ex vivo degradation in blood samples. Clin Biochem 48, 976-981, doi:10.1016/j.clinbiochem.2015.02.014 (2015).
2 Linnarsson, S. Recent advances in DNA sequencing methods – general principles of sample preparation. Exp Cell Res 316, 1339-1343, doi:10.1016/j.yexcr.2010.02.036 (2010).
3 Gaillard, C. & Strauss, F. Avoiding adsorption of DNA to polypropylene tubes and denaturation of short DNA fragments. Technical Tips Online 3, 3 (1998).
Ensure you are using the right concentration of ROX because different instruments require different ROX concentrations. For example, if a qPCRBIO Probe Mix Hi-ROX is used with an instrument requiring a Lo-ROX mix, the software will normalise the qPCRBIO signal against the Hi-ROX level. This will significantly reduce the fluorescence level of the qPCRBIO mix relative to competitors’ mixes, if in that case the Lo-ROX mix was chosen for the competitor.
When comparing mixes from different manufacturers, it is better to carry out separate runs or turn the passive reference off before analysing data.
It’s most likely because the time for the 1st step (hot start) is too short. Ensure that the hot start phase is done at 95°C for 2 minutes to fully activate the enzyme. The recommended thermal profile is:
- 95°C (120 seconds)
- 40 cycles: 95°C (5-15 seconds) – 60°C (20-30 seconds)
- Melt
If non-specific products are still obtained, we recommend raising the annealing/extension temperature from 60°C to 65°C, depending on the primer set used.
Yes, this storage buffer is compatible. The EDTA will chelate some of the magnesium in the mix, but not significantly enough to affect the reaction.
If inhibition is observed, the amount of template in the reaction can be decreased. This will increase the Ct value but lower the likelihood of inhibitors interfering with the Taq DNA polymerase activity. If this doesn’t work, try adding 0.4-4 mg/ml of BSA to the reaction1,2. Ensure the cycling conditions in our product manual are adhered to.
1 Kreader, C. A. Relief of amplification inhibition in PCR with bovine serum albumin or T4 gene 32 protein. Appl Environ Microbiol 62, 1102-1106 (1996).
2 Wilson, I. G. Inhibition and facilitation of nucleic acid amplification. Appl Environ Microbiol 63, 3741-3751 (1997).
Yes. The usual activation time of 2 minutes is not a long enough time to ensure release of the DNA from the bacteria or virus sample. The activation step can be increased to 15 minutes without affecting the reaction yield.
We recommend using 0.4 µM of each primer. There is a degree of flexibility around this recommended concentration however, the primer concentration should not be increased, as this may significantly affect the activity of the enzyme.
Different products could give a different plateau of fluorescence. However, this has no impact on quantification accuracy and Ct values will not differ among products.
There are different options to consider when optimising the reaction:
- Reduce the annealing/extension time to 5 seconds
- Increase the annealing/extension temperature from 60 to 65°C
- Dilute the DNA template by starting with 5ng of DNA and using a 10x template dilution series. In addition to running these on a gel to see if the non-specific products persist, the efficiency of the reaction can be calculated with the software of the qPCR instrument after doing the template dilution. If the efficiency is between 90 – 110%, then the amplicon is being doubled every cycle.
No. Apart from ROX, there is no other dye in our mixes. You can therefore use any fluorophore-conjugated probe for your reaction. Keep in mind that if you’re using qPCRBIO Probe Blue Mixes, refer to Table 1 in the respective product manuals to ensure the blue dye will not interfere with the fluorescence of your fluorophore.


Xem thêm